Diagnostikk
Funksjonsdiagnostikk
TSH er den beste analysen for å påvise primære endringer i thyreoideafunksjon, fordi hypofysen er svært sensitiv for endringer i konsentrasjonen av thyreoideahormoner pga. feedbackreguleringen mellom thyreoidea, hypofyse, og hypothalamus. Ved primær thyreoideasykdom er TSH høy ved hypotyreose, og lav (oftest supprimert) ved hypertyreose.
Måling av fritt T4 (FT4), og ved hypertyreose, fritt-T3 (FT3) vil si noe om graden av funksjonsforstyrrelse. Det er bedre å måle den frie, biologisk aktive fraksjonen av thyreoideahormon fordi den totale konsentrasjonen (total-T4, total-T3) påvirkes av bindekapasiteten i plasma.
Måling av både TSH og FT4 gjør det mulig å fange opp de subkliniske stoffskifteforstyrrelsene og mer sjeldne tilstander (thyreoideahormonresistens, sykdom i hypofyse eller hypothalamus).
TSH, FT4, og FT3 må alltid vurderes mot hverandre og mot klinisk problemstilling! Husk også at referanseområder er orienterende, i den friske befolkningen vil 2,5% av ha lavere og 2,5% ha høyere verdier enn «grensene».
Konsentrasjonen av TSH, FT4 og FT3 kan påvirkes av medikamenter, fysiologiske endringer, sykdom, og medfødte tilstander. De måles med immunoassay og det kan også forekomme interferens. Ta kontakt med laboratoriet ved ulogiske prøvesvar!
Autoimmunitet
Autoimmunitet er den vanligste årsaken til thyreoideasykdommer i Norge. Påvisning av antistoffer er viktig for å stille etiologisk diagnose.
TSH-reseptor antistoffer (TRAS) virker stimulerende (eller hemmende) på TSH-reseptorene i thyreoidea. De kan krysse placenta og påvirke fosteret både under og etter svangerskapet. Stimulerende antistoffer er vanligst, noen laboratorier måler derfor TSI (thyreoidea stimulerende immunglobulin) i stedet for TRAS. TRAS (TSI) brukes differensialdiagnostisk ved hypertyreose, og sees med Graves’ sykdom (> 95% av ubehandlede har økte verdier). Ved behandling med tyreostatika vil vanligvis TRAS (TSI) synke, målbart TRAS (TSI) ved seponering er forbundet med økt risiko for residiv.
Økt konsentrasjon av antistoffer mot tyreoperoksidase (anti-TPO) forekommer ved thyreoiditter (Hashimotos thyreoiditt, postpartum og stum thyreoiditt), men også ved Graves’ sykdom. Anti-TPO-titeret sier ikke noe om alvorlighetsgrad, og kan ikke brukes til å monitorere behandling. Ca. 10% av thyreoideafriske har lett økt anti-TPO, forekomsten er høyere blant kvinner og øker med alderen. Økt anti-TPO er forbundet med økt risiko for å utvikle hypotyreose.
Kreft
Tyreoglobulin (Tg) brukes som tumormarkør i oppfølgingen etter behandling for differensiert (papillær og follikulær) cancer thyreoidea. Anti-Tg må rekvireres samtidig. Ved positiv anti-Tg er ikke Tg-verdien pålitelig. Brukes ikke som screening for kreft. Kalsitonin brukes i diagnostikk og oppfølging av medullær cancer thyreoidea, samt ved utredning av multiple endokrine neoplasier (MEN) og nevroendokrine svulster. Brukes ikke som screening ved knutediagnostikk i allmennpraksis.
Valg av prøver
I første omgang måles prøvene markert i grønt. Hvis det påvises patologiske verdier, tas det ny blodprøve med kontroll av funksjonsprøvene, samt tilleggsprøvene markert i hvitt.
| Problemstillinger i allmennpraksis | TSH | FT4 | FT3 | TRAS | Anti-TPO | Annet |
|---|
| Svak klinisk mistanke om hypotyreose eller hypertyreose | ✔ | | | | | |
| Klinisk mistanke om hypotyreose | ✔ | ✔ | | | ✔ | |
| Klinisk mistanke om hypertyreose | ✔ | ✔ | ✔ | ✔ | | |
| Struma eller knute i thyreoidea* | ✔ | ✔ | | | ✔ | Kalsium |
* Malignitetssuspekte knuter utredes med ultralyd og finnålscytologi på sykehus. I forbindelse med den kirurgiske konsultasjonen tas TSH, FT4, anti-TPO, kalsium, PTH, kalsitonin.
Nyfødtscreening. Medfødt hypotyreose er den hyppigste årsaken til behandlbar mental retardasjon. TSH er inkludert i blodprøven som tilbys alle barn som fødes i Norge (tas vanligvis 48-72 timer etter fødsel). Les mer på Nyfødtscreeningens nettsider.
Nyfødte av mødre med forhøyet TRAS. Barnet vurderes klinisk og med thyreoideaprøver 2 dager og 10-12 dager etter fødselen.
Selektiv screening av gravide. Måling av TSH, FT4 og anti-TPO anbefales ved første svangerskapskontroll hos de med risikofaktorer for thyreoideasykdom. Les mer i Nasjonal Veileder i Endokrinologi.
Screening før oppstart av medikamenter. Noen medikamenter kan gi thyreoideadysfunksjon (amiodarone, interferon, alemtuzumab, litium). Det kan være aktuelt å undersøke thyreoideafunksjon før og i løpet av behandlingen.
Refleksjon
Burde man screene friske voksne for stoffskifteforstyrrelser?
Generell screening for hypotyreose hos asymptomatiske voksne er ikke anbefalt. Det kan derimot være aktuelt hos friske individer med økt risiko for hypotyreose, samt hos de som har andre laboratorie- eller billeddiagnostiske funn som kan tyde på hypotyreose. I allmennpraksis er det greit å ha en lav terskel for å måle TSH: prøven er billig, enkel og lett tilgjengelig, og hypotyreose er en vanlig problemstilling.
Laboratorieverdier ved thyreoideasykdommer
| TILSTANDER | TSH | FT4 | | FT3 | SUPPLERENDE UNDERSØKELSER |
|---|
| Hypotyreose | | | | | |
| Subklinisk (latent) hypotyreose | ↑ <10 mIU/L | n | | | Pasienten er asymptomatisk |
| Primær hypotyreose | ↑ | ↓ | | | |
Autoimmune thyreoiditter- Hashimotos thyreoiditt
- Postpartum thyreoiditt
- Stum thyreoiditt
| ↑ | ↓ | | | Anti-TPO (+) |
| Subakutt thyreoiditt | ↑ | ↓ | | | Anti-TPO (–) |
| Sekundær eller tertiær hypotyreose (sjeldent) | ↓ / n | ↓ | | (↓) | Hypofysefunksjonsprøver, MR/CT caput i regi av endokrinolog |
| Hypertyreose | | | | | |
| Subklinisk (latent) hypertyreose | ↓ | n | | n | Pasienten er asymptomatisk |
| Primær hypertyreose | ↓↓ | ↑ | og/eller | ↑ | |
| T3-tyreotoksikose | ↓↓ | n | | ↑ | |
| Graves’ sykdom | ↓↓ | ↑ | og/eller | ↑ | TRAS (+) |
| Toksisk adenom eller knutestruma | ↓↓ | ↑ | og/eller | ↑ | TRAS (–) Scintigrafi: ett eller flere område(r) med ↑ opptak,
ellers ↓ opptak |
Autoimmune thyreoiditter- Postpartum thyreoiditt
- Stum thyreoiditt
- (Hashimotos thyreoiditt)
| ↓↓ | ↑ | og/eller | ↑ | TRAS (–), ofte anti-TPO (+) Scintigrafi (ikke rutine!): ↓ opptak |
| Subakutt thyreoiditt | ↓↓ | ↑ | og/eller | ↑ | Smerter på halsen, feber, ↑ CRP
TRAS (–), anti-TPO (–) Scintigrafi: ↓ opptak |
| Sekundær hypertyreose (svært sjeldent) | ↑ | ↑ | | | Hypofysefunksjonsprøver, ↑ SHBG, CT/MR caput i regi av endokrinolog |
| Thyreoideahormonresistens (sjeldent) | n / ↑ | n / ↑ | | | Thyreoideahormonresistensanalyse |
↑ = høy; ↓ = lav; ↓↓ = supprimert; n = normal; (+) positiv; (–) negativ.
Detaljerte analysebeskrivelser
| TSH |
| Fritt-T4 |
| Fritt-T3 |
| TRAS (eller TSI) |
| Anti-TPO |
| Anti-Tg |
| Tyreoglobulin (Tg) |
| Kalsitonin |
| Total-T4 og total-T3 (lite brukt) |
Tyroksinbindende globulin (TBG)
(lite brukt) |
Thyreoideahormonresistensanalyse
(lite brukt) |
Klikk på menyen for å se beskrivelsene.
TSH
TSH produseres i hypofysens forlapp og stimulerer syntese og sekresjon av trijodtyronin (T3) og tyroksin (T4) i thyreoidea.
Måling av TSH er aktuelt ved mistanke om hypo- eller hypertyreose og ved kontroll under pågående behandling med thyreoideahormoner (eller tyreostatika, men ikke de første 6-12 mnd).
TSH 0,5 – 3,5 mIU/L (metode- og laboratorieavhengig referanseområde)
Umiddelbart etter fødselen er TSH svært høy. Barn har høyere TSH-verdier enn voksne. Gravide kan ha lavere verdier tidlig i svangerskapet: hCG ligner strukturelt på TSH og kan stimulere thyreoidea. Det gir økt sekresjon av T3 og T4, som gir lavere TSH-utskillelse fra hypofysen. For gravide brukes laboratoriets egne trimesterspesifikke referanseområder.
Endringer i TSH er et sensitivt og spesifikt mål på primære endringer i thyreoideafunksjon. En unormal TSH-verdi må alltid vurderes mot klinikken og serumkonsentrasjon av fritt-T4 (FT4), og fritt-T3 (FT3) ved hypertyreose.
Høy TSH
- Primær hypotyreose: TSH > 10 mIU/L og lav FT4
- Subklinisk hypotyreose: TSH 3,5 – 10 mIU/L, normal FT4, symptomfri
- Partiell thyreoideahormonresistens (sjeldent): normal/lett forhøyet TSH og normal/lett forhøyet FT4, ofte eutyreot
- Sekundær hypertyreose (TSH-produserende tumor i hypofysen, svært sjeldent): høy TSH og høy FT4
- Andre årsaker: fedme, litium, dopaminantagonister (f.eks. metoklopramid), jod i store doser, interferens i målemetoden f.eks. heterofile antistoffer
Lav TSH
- Primær hypertyreose: supprimert TSH, høy FT4 og/eller FT3
- Subklinisk hypertyreose: TSH < 0,5 mIU/L, normal FT4 og FT3, symptomfri
- Sekundær eller tertiær hypotyreose (sykdom i hypofyse eller hypothalamus): normal/lav TSH, lav FT4
- Andre årsaker: graviditet, alvorlig generell sykdom, ubehandlet binyresvikt, glukokortikoider, L-dopa, dopamin, jod i store doser, interferens av enkelte medikamenter og biotin.
Les mer om TSH i Brukerhåndboken i Medisinsk Biokjemi.
Fritt-T4
Tyroksin (T4) produseres i thyreoidea og har en negativ tilbakekoblingseffekt på sekresjon av TSH i hypofysen og TRH i hypothalamus. T4 er bundet til plasmaproteinene tyroksinbindende globulin (TBG), transtyretin (prealbumin) og albumin i blodet. Cirka 0,03% sirkulerer fritt og er biologisk aktiv. Denne fraksjonen kalles fritt-T4 (FT4).
Måling av FT4 benyttes ved diagnostikk av hypo- eller hypertyreose, og ved kontroll av pågående behandling av thyreoideasykdommer. Ved behandling med levotyroksin bør pasienten være medikamentfastende.
FT4 8 – 21 pmol/L (metode- og laboratorieavhengig referanseområde)
Etter fødselen er FT4 høy. Barn har litt høyere FT4-verdier enn voksne. FT4-verdiene kan være lett nedsatte sent i svangerskapet pga. økt konsentrasjon av plasmaproteiner.
FT4 tolkes sammen med TSH og klinikken.
Høy FT4
- Primær hypertyreose: supprimert TSH
- Partiell thyreoideahormonresistens: normal/høy TSH (sjeldent)
- Sekundær hypertyreose (TSH-produserende tumor i hypofysen): høy TSH (svært sjeldent)
Lav FT4
- Primær hypotyreose: høy TSH
- Sekundær eller tertiær hypotyreose (sykdom i hypofyse eller hypothalamus): normal/lav TSH (sjeldent)
Ved ulogiske prøvesvar bør man kontakte laboratoriet, da feilmålinger kan skyldes interferens (biotin, heterofile antistoffer, endogene T4-bindende antistoffer, assay-artefakter).
Måling av FT4 skal vanligvis ikke påvirkes av bindingskapasiteten i blodet, men enkelte analysemetoder kan gi feilmålinger. Frie fettsyrer og noen medikamenter (salisylater, NSAIDs, furosemid, heparin, fenytoin, karbamazepin) kan endre plasmaproteinenes evne til å binde T4. Mengden tyroksinbindende globulin (TBG) øker ved graviditet og bruk av p-piller, og den faller ved alvorlig sykdom, leversvikt, nefrotisk syndrom og bruk av glukokortikoider.
Les mer om fritt-T4 i Brukerhåndboken i Medisinsk Biokjemi.
Fritt-T3
Trijodtyronin (T3) produseres i thyreoidea eller dannes ved dejodering av tyroksin (T4) i perifere vev. T3 har en negativ tilbakekoblingseffekt på sekresjon av TSH i hypofysen og TRH i hypothalamus. T3 er bundet til plasmaproteinene tyroksinbindende globulin (TBG), transtyretin og albumin i blodet. Cirka 0,3% sirkulerer fritt og er biologisk aktiv. Denne fraksjonen kalles fritt-T3 (FT3).
Måling av FT3 benyttes ved diagnostikk av hypertyreose. Ved behandling med liotyronin bør pasienten være medikamentfastende.
FT3 2,8 – 7,0 pmol/L (metode- og laboratorieavhengig referanseområde)
FT3 tolkes sammen med TSH, FT4 og klinikken.
Høy FT3
- Hypertyreose: supprimert TSH, høy FT4. Normal/lav FT4 kan tyde på selektiv overproduksjon av T3 (T3-tyreotoksikose).
- Partiell thyreoideahormonresistens: normal/høy TSH (sjeldent)
Lav FT3
- Hypotyreose: høy TSH (men måling av FT3 har ingen/liten plass i diagnostikk av hypotyreose!)
- Ikke-tyreoidal sykdom: ved alvorlig stress eller generell sykdom er dejoderingen av T4 til T3 hemmet
Ved ulogiske prøvesvar bør man kontakte laboratoriet, da feilmålinger kan skyldes interferens (biotin, heterofile antistoffer, endogene T3-bindende antistoffer, assay-artefakter).
Måling av FT3 skal vanligvis ikke påvirkes av bindingskapasiteten i blodet, men enkelte analysemetoder kan gi feilmålinger. Frie fettsyrer og noen medikamenter (salisylater, NSAIDs, furosemid, heparin, fenytoin, karbamazepin) kan endre plasmaproteinenes evne til å binde T3. Mengden tyroksinbindende globulin (TBG) øker ved graviditet og bruk av p-piller, og den faller ved alvorlig sykdom, leversvikt, nefrotisk syndrom og bruk av glukokortikoider.
Les mer om fritt-T3 i Brukerhåndboken i Medisinsk Biokjemi.
TRAS (eller TSI)
TSH-reseptor antistoffer (TRAS) kan virke stimulerende eller blokkerende på TSH-reseptorene i thyreoidea. TRAS er et IgG som kan krysse placenta og påvirke fosteret både under og etter svangerskapet. Stimulerende antistoffer er vanligst, og noen laboratorier måler TSI (thyreoideastimulerende immunoglobulin) i stedet for TRAS.
Stimulerende antistoffer gir økt syntese og sekresjon av tyroksin (T4) og trijodtyronin (T3), og follikkelcellevekst (struma). Blokkerende antistoffer gir nedsatt syntese og sekresjon av T4 og T3, og thyreoidea kan atrofiere.
Måling av TRAS (eller TSI) er indisert ved:
- Differensialdiagnostikk av hypertyreose
- Kontroll av Graves’ sykdom (ikke nødvendig å måle underveis i behandlingen)
- Graviditet hos kvinner behandlet for Graves’ sykdom (med radioaktivt jod eller kirurgi), med aktiv Graves’ sykdom, eller som tidligere har født barn med neonatal hypertyreose
- Diagnostikk av neonatal hyper- eller hypotyreose
- Mistanke om endokrin oftalmopati
TRAS (eller TSI) negativ (metode- og laboratorieavhengig referanseområde)
TRAS (eller TSI) tolkes sammen med klinikk og funksjonsanalyser (TSH, fritt-T4 og fritt-T3).
Positiv TRAS (eller TSI): Sammen med klinisk og biokjemisk hypertyreose er det diagnostisk for Graves’ sykdom.
Høy TRAS (eller TSI) ved avslutning av behandling for Graves’ sykdom indikerer større risiko for residiv.
Gravide med TRAS (eller TSI) 3x høyere enn øvre referansegrense bør henvises til fostermedisiner og endokrinolog.
Biotin kan skape interferens og gi et falsk positivt resultat.
Les mer om TRAS i Brukerhåndboken i Medisinsk Biokjemi.
Anti-TPO
Anti-TPO er autoantistoffer rettet mot enzymet tyreoperoksidase (TPO) i follikkelcellene i thyreoidea. Anti-TPO er en markør på en autoimmun prosess.
Måling av anti-TPO er aktuelt ved utredning av hypotyreose, subklinisk hypotyreose og struma, samt ved bruk av medikamenter som kan påvirke immunforsvaret eller thyreoidea (amiodarone, interferon, alemtuzumab, litium). Konsentrasjon av anti-TPO endrer seg lite over tid og brukes ikke for å overvåke behandlingseffekt.
Anti-TPO negativ (metode- og laboratorieavhengig referanseområde)
Anti-TPO tolkes sammen med klinikk og funksjonsanalyser (TSH, fritt-T4).
Positiv anti-TPO: Typisk for Hashimotos thyreoiditt, post partum thyreoiditt, og stum autoimmun thyreoiditt. Kan være økt ved Graves’ sykdom (hypertyreose). Omtrent 10% av thyreoideafriske har lett økt anti-TPO, forekomsten er høyere blant kvinner og øker med alderen. Økt anti-TPO er forbundet med økt risiko for å utvikle hypotyreose.
Les mer om Anti-TPO i Brukerhåndboken i Medisinsk Biokjemi.
Anti-Tg
Tyreoglobulin (Tg) syntetiseres i follikkelcellene i thyreoidea og inngår i syntesen og lagringen av thyreoideahormonene. Tg er antigent og trigger lett immunapparatet. Autoantistoffer mot tyreoglobulin (anti-Tg) trenger ikke være en markør på en autoimmun prosess. Ved mistanke om autoimmun thyreoiditt skal man heller måle autoantistoffer mot tyreoperoksidase (anti-TPO). Anti-Tg verdien gir liten/ingen klinisk informasjon.
Måling av anti-Tg er viktig i oppfølging av differensiert (papillær og follikulær) thyreoideakreft fordi Tg brukes som tumormarkør. Tilstedeværelse av anti-Tg kan interferere og gi falske lave Tg-verdier.
Anti-Tg negativ (metode- og laboratorieavhengig referanseområde)
Positiv anti-Tg: Måling av Tg kan verdien være falsk lav. Skifte fra negativ til positiv anti-Tg i løpet av oppfølgingen for differensiert thyreoideakreft kan tyde på restsykdom eller residiv. Ca. 10% av befolkningen har positiv anti-Tg, men det er ikke assosiert med økt risiko for hypotyreose (som ved positiv anti-TPO).
Les mer om Anti-Tg i Brukerhåndboken i Medisinsk Biokjemi.
Tyreoglobulin (Tg)
Tyreoglobulin (Tg) produseres bare i follikkelcellene i thyreoidea og inngår i syntesen og lagringen av thyreoideahormonene tyroksin (T4) og trijodtyronin (T3). Må ikke forveksles med plasmaproteinet tyroksinbindende globulin (TBG) som produseres i leveren!
Tg er en thyreoideaspesifikk tumormarkør som brukes i oppfølgingen etter behandling for differensiert (papillær og follikulær) cancer thyreoidea. Anti-Tg må alltid rekvireres samtidig. Analysen skal ikke brukes til screening av kreft.
Tyreoglobulin < 30 μg/L (metode- og laboratorieavhengig referanseområde)
Konsentrasjonen av Tg avhenger av mengden thyreoideavev og grad av TSH-stimulering.
Høy Tg: Hvis Tg er målbar (etter total fjerning eller ablasjon av thyreoidea) eller stiger (etter hemithyreoidektomi) tyder det på restsykdom, metastase eller residiv av differensiert cancer thyreoidea. Andre årsaker: thyreoiditt, tyreotoksikose, struma, radiojodbehandling, kirurgi eller biopsi av thyreoidea.
Lav Tg: Thyreotoxicosis factitia eller medfødt agenesi av thyreoidea (sjeldent). Anti-Tg kan interferere og gi falsk lav Tg.
Les mer om Tyreoglobulin i Brukerhåndboken i Medisinsk Biokjemi.
Kalsitonin
Kalsitonin er et peptidhormon som produseres i de parafollikulære cellene i thyreoidea (C-cellene). Kalsitonin stimuleres av hyperkalsemi og gastrin, og senker kalsiumkonsentrasjonen i blodet ved å hemme osteoklastenes frigjøring av kalsium og fosfat fra bein, samt ved å øke utskillelsen av kalsium og fosfat i nyrene. Effekten av kalsitonin er fortsatt noe uavklart.
Måling av kalsitonin er aktuelt i både diagnostikk og oppfølging av medullær thyreoideakreft, samt ved utredning av multiple endokrine neoplasier (MEN) og nevroendokrine svulster.
| Kalsitonin | kvinner | < 1,6 pmol/L (metode- og laboratorieavhengig referanseområde) |
| menn | < 2,2 pmol/L (metode- og laboratorieavhengig referanseområde) |
Høy kalsitonin:
- Medullær thyreoideakarsinom (MTC). Høy eller stigende kalsitonin etter behandling for MTC tyder på restsykdom, metastase eller residiv.
- Nevroendokrine svulster i GI-traktus og bronkiene, noen former for lunge-, bryst- og pankreaskreft, samt ved nyresvikt, hyperkalsemi, og hypergastrinemi.
- (Autoimmun thyreoiditt)
Lav kalsitonin: Thyreoidektomerte pasienter har vanligvis kalsitonin < 0,6 pmol/L
Hemolyse kan gi falskt høye verdier.
Les mer om Kalsitonin i Brukerhåndboken i Medisinsk Biokjemi.
Total-T4 og total-T3
I noen spesielle situasjoner kan det være aktuelt å måle totalmengden av tyroksin (T
4) og trijodtyronin (T
3) i blodet. Det vil si både den frie fraksjonen som er biologisk aktivt, og det som er bundet til bindeproteiner som TBG (tyroksinbindende globulin), prealbumin (transtyretin) og albumin. Måling av fritt-T
4 og fritt-T
3 er ellers best for å vurdere stoffskiftet.
Les mer om total-T3 i Brukerhåndboken i Medisinsk Biokjemi. Les mer om total-T4 i Brukerhåndboken i Medisinsk Biokjemi.
Tyroksinbindende globulin (TBG)
Tyroksinbindende globulin (TBG) er et plasmaprotein som produseres i leveren. Må ikke forveksles med tyreoglobulin (Tg) som produseres i thyreoidea!
Måling av TBG benyttes sjeldent, men er relevant ved mistanke om medfødt TBG-mangel eller unormale konsentrasjoner av total-T4 eller total-T3 (som regel ikke fritt-T4 og fritt-T3).
TBG 14 - 31 mg/L (metode- og laboratorieavhengig referanseområde)
Høy TBG: Graviditet, hepatitt, porfyri, medfødte tilstander, bruk av medikamenter som p-piller, østrogener, heroin, metadon, perfenazin (antipsykotikum), selektive østrogenreseptormodulatorer (f.eks. tamoksifen), 5-fluorouracil (cytostatikum), mitotan (cytostatikum).
Lav TBG: Akutt generell sykdom, leversvikt, nefrotisk syndrom, medfødte tilstander, bruk av medikamenter som glukokortikoider, androgener, anabole steroider, L-asparaginase (cytostatikum), niacin.
Les mer om Tyroksinbindende globulin i Brukerhåndboken i Medisinsk Biokjemi.
Thyreoideahormonresistensanalyse
Thyreoideahormonresistens forekommer hos 1 av 50 000, nedarves autosomalt dominant, og skyldes oftest en mutasjon i genet for thyreoideahormonreseptor beta (TR-β). Pasientene har en partiell hormonresistens (ettersom en total resistens er uforenelig med liv), kan ha struma, og er oftest klinisk eutyreote. Noen kan ha uspesifikke symptomer på hypo- eller hypertyreose. Fritt-T
4 og fritt-T
3 er lett til moderat forhøyet, men TSH er ikke supprimert, heller i øvre del av referanseområdet, evt. lett forhøyet.
Analysen bestilles ved mistanke om thyreoideahormonresistens, men man bør utelukke interferens og TSH-produserende hypofysetumor først. Fordi mange forskjellige mutasjoner kan gi resistens må hele genet sekvenseres, med mindre en mutasjon har blitt påvist tidligere i samme familie.
Les mer om Thyreoideahormonresistensanalyse i Brukerhåndboken i Medisinsk Biokjemi.
Trippeldiagnostikk krever spesialisert og tverrfaglig kompetanse, og inkluderer:
- Klinisk undersøkelse og blodprøver
- Ultralyd av halsen
- Ultralydveiledet finnålscytologi ved behov
Flytskjemaet nedenfor illustrerer prosessen ved knutediagnostikk.
Trykk på  og
og  for å vise/skjule ytterligere informasjon.
for å vise/skjule ytterligere informasjon.
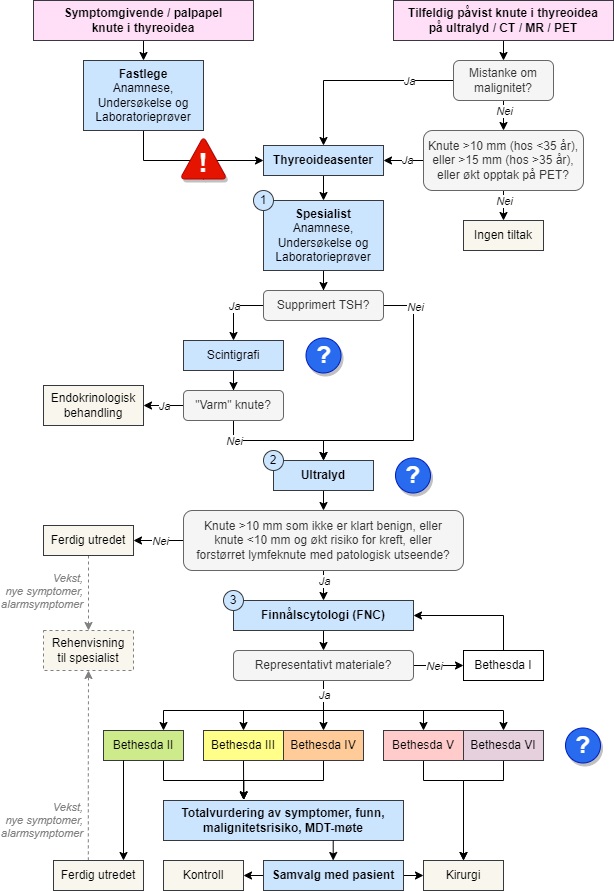
Rask henvisning ved mistanke om kreft:
Alarmsymptomer
Palpabel knute og minst ett av følgende:
- Rask vekst
- Fiksering til omgivende vev
- Nyoppstått heshet
- Nyoppståtte svelge- og pustevansker
- Nyoppståtte smerter
- Blodig hoste
Pasienter under 18 år
Spesielle ultralydfunn eller celleforandringer
Scintigrafi kan utelukke et hyperfungerende adenom, en såkalt «varm knute». Disse er nesten alltid godartede og kan behandles med radioaktivt jod, kirurgi eller tyreostatika.
Ultralyd er best for å undersøke knuter i thyreoidea. Funn må ses i sammenheng med pasientens risikofaktorer, klinikk og blodprøver. Man kan bruke et TIRADS for å rapportere funn og vurdere behov for finnålscytologi og oppfølging.
| Bethesda-gruppe | Malignitetsrisiko | Anbefalt oppfølging |
|---|
| I. Ikke diagnostisk, uegnet | 1-4% | Ny ultralydveiledet FNC |
| II. Benign | 0-3% | Ofte ferdig utredet, kontroll ved behov |
| III. Irregulære celler eller follikulær lesjon med usikker betydning | 5-15% | Kontroll med ny ultralydveiledet FNC |
| IV. Follikulær neoplasi eller suspekt på follikulær neoplasi | 15-30% | Vanligvis kirurgi |
| V. Mistanke om malignitet | 60-75% | Kirurgi |
| VI. Malign | 97-99% | Kirurgi |
| Nukleærmedisin | Ultralyd | CT | MR |
|---|
| Indikasjoner | Hypertyreose med negativ TRAS (eller TSI).
Knute(r) og supprimert TSH.
Doseberegning før radiojodbehandling.
Utredning av medfødt hypotyreose.
| Palpabel knute i thyreoidea.
Voksende knutestruma.
Forstørrede regionale lymfeknuter.
Mistanke om malignitet.
Utredning av medfødt hypotyreose.
| Endokrin oftalmopati.
Mistanke om intrathorakalt struma.
Vurdering av tumorutbredelse, sykdomsstadium, og operabilitet.
| Endokrin oftalmopati.
Vurdering av tumorutbredelse, sykdomsstadium, og operabilitet.
|
⊕ Fordeler
⊖ Ulemper
|
- ⊕
- Fremstiller funksjon.
- ⊕
- «Varme» knuter er nesten alltid benigne.
- ⊖
- «Kalde» knuter kan ikke vurderes for malignitet.
- ⊖
- Gir ikke en presis anatomisk fremstilling.
- ⊖
- Kontraindisert ved graviditet, forsiktighetsregler ved amming.
- ⊖
- Påvirkes av jodholdige kontrastmidler, medisiner og kosttilskudd inntatt de siste 2-4 måneder.
- ⊖
- Ioniserende stråler.
|
- ⊕
- God fremstilling av anatomi, særlig thyreoidea og lymfeknuter.
- ⊕
- God fremstilling av benigne og maligne trekk.
- ⊕
- Farge-Doppler kan fremstille blodsirkulasjon.
- ⊕
- Kan veilede finnålsbiopsi.
- ⊖
- Vanskelig å fremstille strukturer som ligger dypt eller bak luft og ben.
- ⊖
- Avhengig av kompetent undersøker.
|
- ⊕
- God fremstilling av anatomi, særlig relasjonen til tilgrensende organer.
- ⊕
- Tilgjengelig, lite ressurskrevende.
- ⊖
- Kontrastmiddel påvirker utredning og behandling med radiojod i minst 2 måneder.
- ⊖
- Kontrastmiddel kan gi bivirkninger.
- ⊖
- Ioniserende stråler.
|
- ⊕
- God fremstilling av anatomi, særlig bløtdeler.
- ⊖
- Ressurskrevende, lite tilgjengelig.
- ⊖
- Kontrastmiddel kan gi bivirkninger.
- ⊖
- Kontraindisert ved metall i kroppen (klips, implantater, pacemaker…).
|
Nukleærmedisin
Virkningsmekanisme. Pasienten får en spormengde av radioaktivt merket stoff (= tracer) som fordeler seg i kroppen og oppkonsentreres i organet man ønsker å undersøke, uten å forstyrre de metabolske prosessene det inngår i. Ved undersøkelse av thyreoidea brukes 99mTc-perteknetat eller radioaktivt jod (131I eller 123I). Disse transporteres inn thyreoideas follikkelceller gjennom Na+/I- symportere (NIS), på samme måte som jodid, men 99mTc-perteknetat inngår ikke i hormonsyntesen.
Gammastråler fra det radioaktive stoffet registreres med et spesielt kamera og det dannes et todimensjonalt bilde, kalt scintigram. Teknikken SPECT (= Single Photon Emission Computed Tomography) gjør det mulig å registrere stråling i flere snittplan og lage en tredimensjonal rekonstruksjon som kan kombineres med CT.
Tolkning. Normalt ser man et rimelig homogent og symmetrisk opptak av tracer i hele kjertelen, et perteknetatopptak på 0,5% – 3,5% av injisert dose, og en kjertelvekt på ca. 15 gram (øvre normale normalgrense er 25 gram). De scintigrafiske undersøkelsene suppleres med opplysninger om den kliniske problemstillingen og laboratorieverdier.
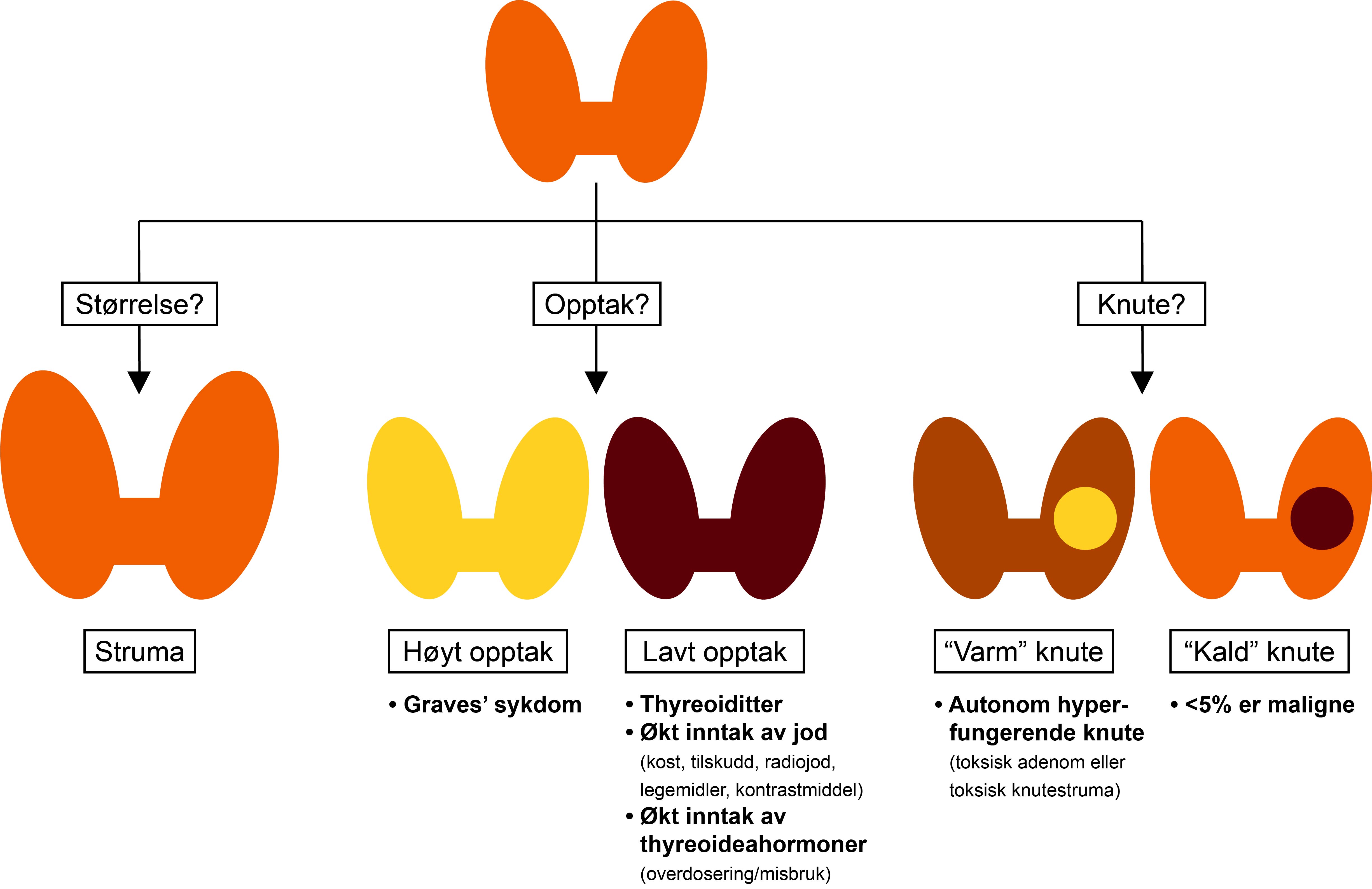
Kilde: Martin Biermann, UiB. Bearbeidet med tillatelse.
Miniquiz
Ultralyd
En thyreoideakompetent radiolog, endokrinkirurg eller ØNH-lege utfører ultralyd av halsen. Knuter i thyreoidea vurderes basert på størrelse, form, innhold, ekkogenisitet, avgrensning, og om det foreligger typisk benigne eller maligne tegn. Med Farge-Doppler kan man se på vaskularisering. Det hører alltid med å undersøke og karakterisere regionale lymfeknuter. En samlet vurdering av ultralydfunnene, risikofaktorer, klinikk, og blodprøver danner grunnlag for videre tiltak, inkludert om det tas finnålscytologi.
Identifiser strukturene ved å trekke navnene til riktig sted på ultralydbildet:
Kilde: Brun VH, Håskjold OI. Standard for diagnostikk av knuter i thyreoidea. Kirurgen. 2019; 3: 208-212. Gjengitt med tillatelse fra Vegard Heimly Brun og Olav Inge Håskjold.
Internasjonalt er det utviklet hjelpemidler kalt TIRADS (Thyroid Imaging Reporting and Data Systems) som kan standardisere utredning og dokumentasjon, samt bidra til å redusere overdiagnostikk og -behandling. Systemene sorterer knutene i risikogrupper basert på ultralydkriterier (se bilde nedenfor), og gir anbefalinger for oppfølging og finnålscytologi.
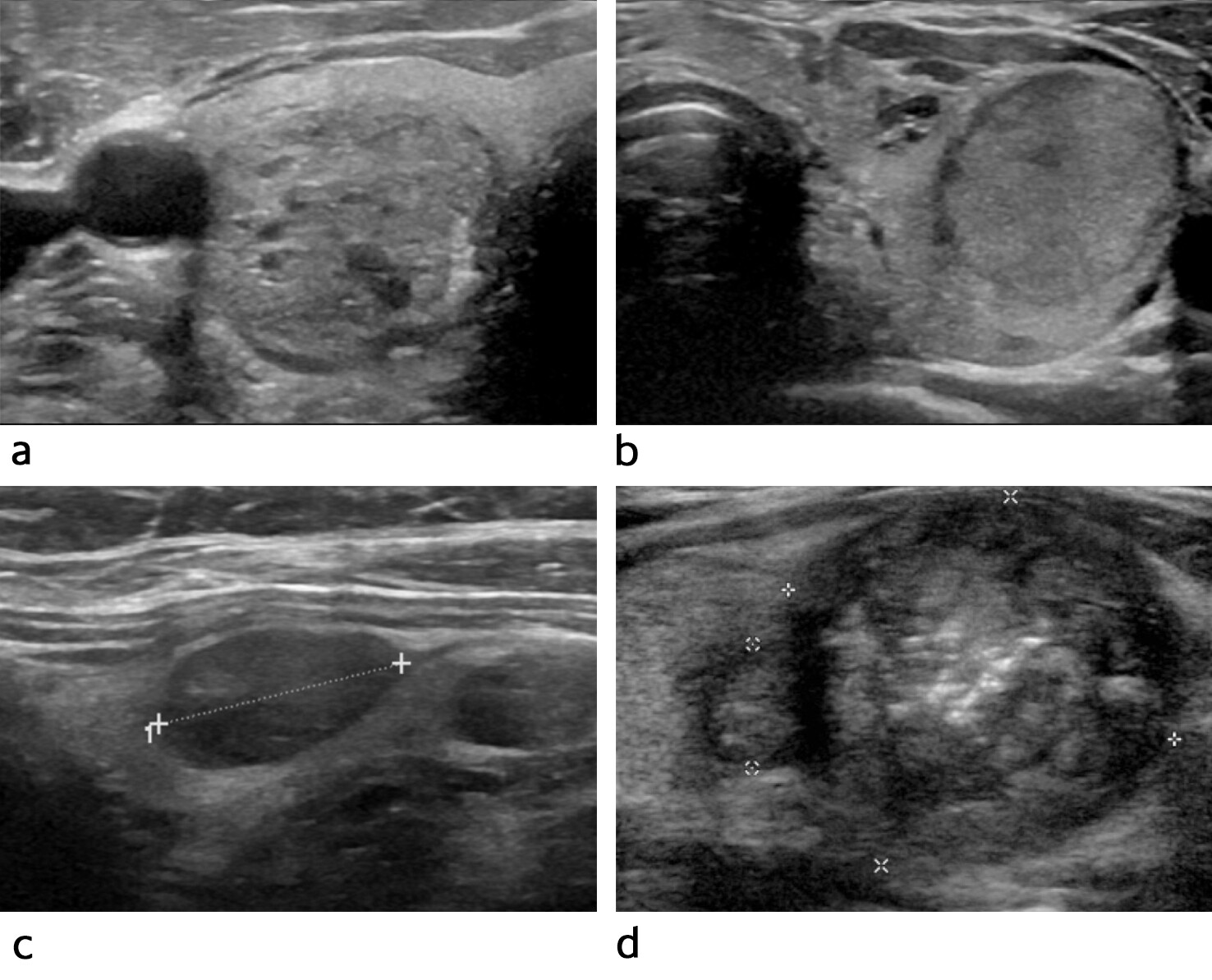
Kilde: Tangerud Å, Sigstad E, Fagerlid KH, Paulsen TH, Norheim I. Knuter i tyreoidea – utredning og oppfølging. Tidsskr Nor Legeforen. 2020; 140(12): 1250–4. Hentet fra: https://doi.org/10.4045/tidsskr.20.0186. Lisensiert under CC BY-ND 4.0.
Typiske ultralydfunn ved ulike klassifiseringer av risiko for malignitet i thyreoidea (TIRAD = Thyroid Imaging Reporting and Data System).
- a)
- Knuten er oval, velavgrenset og svampaktig. Den har et benignt preg (TIRAD 2).
- b)
- Knuten er oval, velavgrenset og isoekkoisk. Det er lav risiko for kreft (TIRAD 3).
- c)
- Knuten er oval, velavgrenset og moderat hypoekkoisk. Det er moderat risiko for kreft (TIRAD 4).
- d)
- Knuten er uskarpt avgrenset, inneholder mikrokalk og er markert hypoekkoisk perifert. Det er høy risiko for kreft (TIRAD 5).
Finnålscytologi er den beste teknikken for å vurdere tumor i thyreoidea. Ved behov kan det gjøres grovnålsbiopsi eller åpen biopsi.
Ultralydveiledet finnålscytologi (FNC) gjøres ved:
- Knuter i thyreoidea > 10 mm som ikke er klart benigne
- Knuter i thyreoidea ≤ 10 mm og økt risiko for kreft (familiær risiko, tidligere strålebehandling, malignitetssuspekte funn på ultralyd)
- Lymfeknuter som er patologisk forstørret og med patologisk utseende (rund, ikke bønneformet, utvisket fetthilus, økt vaskularisering)
Prøvematerialet som høstes kan brukes til:
- Direkte utstryk på objektglass. Noen lufttørkes og hurtigfarges. De kan vurderes raskt av en cytolog (såkalt ROSE = Rapid On-Site Evaluation), og ved behov kan mer materiale innhentes i samme konsultasjon. Andre utstryk fikseres og farges senere.
- Væskebasert cytologi som kan prepareres som utstryk, cytospin eller cytoblokk.
Cytologen ser på kolloid, celletyper, cellularitet, arkitektur og vekstmønster, cellemorfologi, kjerneforandringer og mitoser. Kapsel- eller karinnvekst kan ikke vurderes! Supplerende undersøkelser som immuncytokjemi, immunhistokjemi, molekylærgenetiske analyser (bl.a. BRAF-mutasjonsanalyse mtp. papillært thyreoideakarsinom) og flowcytometrisk immunfenotyping (mtp. lymfom) kan hjelpe i diagnostikken.
Bethesda-systemet brukes for å rapportere cytologiske funn og veilede videre tiltak.
| Bethesda-gruppe | Malignitetsrisiko | Anbefalt oppfølging |
|---|
| I. Ikke diagnostisk, uegnet | 1-4% | Ny ultralydveiledet FNC |
| II. Benign | 0-3% | Kontroll ved behov. Mange er ferdig utredet, men kan rehenvises ved vekst, nye symptomer eller alarmsymptomer |
| III. Irregulære celler eller follikulær lesjon med usikker betydning | 5-15% | Kontroll med ny ultralydveiledet FNC, f.eks. etter 6-12 måneder |
| IV. Follikulær neoplasi eller suspekt på follikulær neoplasi | 15-30% | Vanligvis kirurgi, evt. kontroll med ny ultralydveiledet FNC, f.eks. etter 6-12 måneder |
| V. Mistanke om malignitet | 60-75% | Kirurgi |
| VI. Malign | 97-99% | Kirurgi |

 for å vise/skjule ytterligere informasjon.
for å vise/skjule ytterligere informasjon.

